domingo, 30 de marzo de 2014
sábado, 29 de marzo de 2014
viernes, 28 de marzo de 2014
Fisiopatología del Metabolismo de la Bilirrubina
3.Metabolismo Bilirrubina y Enfermedades from Fernando Costa on Vimeo.
Todos los créditos Dr. Luíz Toledo
Marcadores:
bazo,
bilirrubina,
Bioquímica,
crigler,
directa,
dubin,
gilbert,
Hepática,
Hígado,
hiperbilirrubinemia,
Ictericia,
indirecta,
johnson,
Medicina,
médicos,
metabolismo,
najjar,
patología,
retículo
miércoles, 26 de marzo de 2014
Trypanosoma spp.
Introducción
Las tripanosomosis humanas son producidas por protozoos flagelados que viven en la sangre y tejidos del huésped humano, y son transmitidas por artrópodos hematófagos.
Existen dos enfermedades distintas con localizaciones geográficas diferentes: la americana y la africana.
TRYPANOSOMA BRUCEI
La tripanosomosis africana es causada por hemoprotozoarios flagelados: Trypanosoma brucei gambiense en África Central y Occidental, y Trypanosoma brucei rhodesiense en África Oriental y del Sudeste. Ambas (subespecies de Trypanosoma brucei) pasan parte de su ciclo biológico como parásito en la sangre de los seres humanos y de otros mamíferos. Les produce una enfermedad neurológica fatal, la tripanosomosis, cuyo estadio final en la personas es la enfermedad del sueño.
Agente etiológico, morfología y ciclo de vida
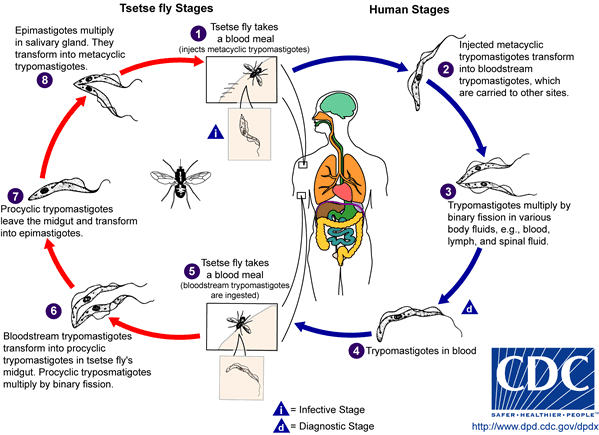
En la actualidad los agentes causales de la tripanosomosis africana, Trypanosoma brucei rhodosiense (Stephens y Fanthan, 1910) y Trypanosoma brucei gambiense (Dutton, 1902), se consideran como subespecies de Trypanosoma brucei, especie patógena para los animales, pero no para el hombre. Por sus diferencias morfológicas en la sangre de los vertebrados, se dice que este tripanosoma es polimorfo: algunos son largos y delgados; otros son cortos, anchos y sin flagelos; y otros intermedios. Tienen movimiento rápido y llegan a medir entre 15 a 40 µm de longitud. El tripomastigote tiene un núcleo central extracelular y un flagelo libre en la parte posterior. Presenta una membrana ondulante y un flagelo libre en la parte anterior. En preparaciones coloreadas, se observan ciertas granulaciones que se tiñen de azul pálido y se conocen como gránulos de volutina.
Existen otros detalles que nos permiten diferenciar ambas formas infectantes: T.b. gambiense es más adaptable a los humanos y es difícil hacerla crecer en animales de laboratorio; mientras T.b rhodesiense es más virulenta para el humano e infecta animales de laboratorio con facilidad. Además es frecuente observar polimorfismo en la infección por T.b rhodesiense y menos en T.b gambiense.
En la evolución de T. brucei y las subespecies parásitas del hombre, hay un huésped vertebrado (ganado doméstico y el hombre) y un huésped invertebrado (mosca hematófaga del género Glossina: tsetsé), que se infecta al picar a una persona o a un animal que tiene en su sangre al parásito. Una vez ingerido los tripomastigotes, se reproducen activamente en el intestino medio y posterior de los insectos y toman forma de epimastigotes; en un lapso de 20 a 40 días emigran a las glándulas salivales, en especial a los conductos. En este sitio se adhieren al epitelio, se dividen nuevamente y en otra picadura de la mosca son transmitidas al hombre o a un animal susceptible. En el huésped vertebrado, los tripomastigotes se multiplican por división binaria en la sangre y los tejidos. Después de infectada la mosca, permanece así por el resto de su vida (hasta 11 meses)
Patología
En el sitio de la picadura de la mosca se produce una reacción inflamatoria localizada, parecida a un furúnculo, que dura de 1 a 2 semanas. Los parásitos invaden la sangre circulante con parasitemia muy notoria. Posteriormente hay invasión a los ganglios linfáticos, donde se produce reacción inflamatoria y proliferación de células endoteliales; la infiltración leucocitaria es de localización presvascular y finalmente en los ganglios se produce fibrosis.
El hígado y el bazo aumentan de tamaño y se vuelven congestivos con infiltrado reticuloendotelial. Después de 3 meses más, el parásito llega al SNC y se produce una meningoencefalitis difusa con edema cerebral y pequeñas hemorragias. En el microscopio se pueden observar proliferación de las neuroglias y células mononucleadas.
El líquido cefalorraquídeo está turbio con proteínas aumentadas y abundantes células mononucleadas. Se pueden hallar parásitos en el tejido subyacente.
Manifestaciones clínicas
En el sitio de la picadura de la mosca, se produce una reacción inflamatoria indurada y dolorosa (chancro de inoculación); luego de un periodo de incubación de 1 a 3 semanas aparecen las primeras manifestaciones clínicas de la enfermedad que se van instalando lenta pero progresivamente.
El período agudo de la enfermedad se caracteriza por un aumento de la parasitemia, seguido de fiebre, astenia, cefalea, dolores articulares, calambres musculares y, algunas veces, eritemas papulares. Entre los episodios febriles, hay períodos libres de síntomas, de hasta 2 semanas de duración. Los ganglios linfáticos crecen (aparecen en 75% de los pacientes), en especial los del cuello, submaxilares y mesentéricos; son móviles y blandos, pero después se tornan duros y fibróticos. El crecimiento de los ganglios linfáticos cervicales posteriores le da al cuello un ensanchamiento característico, que se conoce como el signo de Winterbotton o de lesión invernal, típico de la tripanosomosis por T.b gambiense, lo que no ocurre en T.b rhodesienese ya que esta linfadenopatía cervical es parte complementaria de la linfadenopatía generalizada.
En esta etapa puede observarse hepatomegalia y esplenomegalia. Es frecuente el edema periférico, pulmonar, derrame pleural y pericardico y la neumonía intercurrente. Puede aparecer cardiopatía y causar insuficiencia cardíaca y congestión pulmonar. En la fase crónica de la enfermedad, hay toma del SNC y el cuadro clínico es de una meningoencefalitis, que se instala lenta y progresivamente.
La cefalea es intensa, aparecen insomnio, bulimia, anorexia, coreoatetosis, hiper hipotonía, epilepisia o dificultad en la coordinación motora, incluyendo marcha anormal y ataxias. Es común encontrar hiperreflexia o que sean anormales los reflejos de Babinski, Hoffmann y otros del tallo cerebral arcaico. Hay manifestaciones sensoriales como hiperestesia (signo de Kérandel), y cambios mentales como depresión o euforia.
Todas estas manifestaciones que caracterizan a la enfermedad imposibilitan al paciente hasta para comer, lo que provoca desnutrición severa. Finalmente el enfermo entra en coma profundo y muere por paro respiratorio, para cardíaco o infecciones intercurrentes. Cuando no reciben tratamiento, las dos formas de enfermedad del sueño son mortales. En la subespecie T.b rhodesiense la muerte ocurre casi siempre entre 3 a 6 meses después de iniciada la enfermedad.
Diagnóstico
Para el diagnóstico clínico se toma en cuenta si el enfermo procede de una zona endémica y si fue picado por la mosca setsét.
El diagnóstico de laboratorio se basa en lo métodos directo e indirecto. Entre los directos se hallan: examen de sangre en fresco, tinción de frotis y gota gruesa con Giemsa del LCR, médula ósea y aspirado del chancro inicial o del ganglio linfático. Cuando no es posible visualizar el parásito, se pueden emplear cultivos o inoculaciones a roedores o primates. Existe métodos de concentración por centrifugación o ultrafiltración. Como métodos indirectos, la inmunofluorescencia indirecta es el método indirectos, la inmunofluorescencia indirecta es el método serológico más empleado y la reacción de inmunoprecipitación en gel, en sangre o en el LCR, para investigar anticuerpos IgM específicos. En los casos crónicos, además de la búsqueda del parásito en LCR, se deben observar otras alteraciones, como es el aumento de las células, en especial las monocleadas.
Epidemiología y prevención
Unos 50 000 000 de personas corren el riesgo de contraer la enfermedad. Cada año se contabilizan unos 20 000 casos nuevos. Aún más importante que el reto directo a los seres humanos, lo que es el hecho de que los animales domésticos sean susceptibles a la tripanosomosis, lo que constituye un serio problema en el desarrollo de la industria agropecuaria.
La enfermedad está limitada al continente africano, por la existencia de los vectores apropiados: T.b rhodesiense es transmitida fundamentalmente por Glossina morsitans, que tiene su hábitat en las sabanas de la parte oriental de África Central y Occidental.
Las moscas del género Glossina se identifican principalmente por poseer proboscis picadora, tanto en los machos como en las hembras, Las picaduras ocurren durante las horas de día; y las moscas pueden ser diferenciadas, a pesar de ser en forma y tamaño similares a las moscas domésticas, por la presencia de una celda discal en las alas, que tiene la forma de hacha de carnicero.
Esta moscas son vivíparas, producen larvas maduras que forman ninfas una vez que las larvas ha sido enterradas en suelo arenoso. Requieren de humedad, sombra y temperatura promedio entre 20 y 30°C, además de la presencia de mamíferos como fuente de alimentos; son capaces de volar hasta 20 km en busca de alimento.
Tratamiento
Actualmente se combate la mosca tsetsé, y se trata de modificar su entorno ecológico con la tala de los árboles y vegetación, el uso de insecticidas y el tratamiento de los reservorios, tanto humanos como animales. Como profilaxis individual se utilizan los repelentes.
La mayoría de las drogas utilizadas para combatir la enfermedad no es efectiva y, además produce reacciones secundarias tóxicas y severas; sin embargo, reducen la mortalidad y previenen los daños neurológicos si son administradas al comienzo de la infección, cuando no haya invadido el SNC.
Drogas de elección
Suramina. En la fase aguda de la enfermedad, antes de la encefalitis, comprobada con LCR normal, se aplica por vía endovenosa a la dosis de 4mg/Kg el primer día; 10mg/kg el ter día; 20mg/kg los días 7; 14 y 21 sin pasar de 1g. La suramina tiene algunos efectos secundarios como náuseas, vómitos, convulsiones y estado de choque.
Melarsoprol. Se administra cuando ya existe compromiso del SNC. Se recomiendan de 2 a 3,6 mg/kg/día dividida en tres dosis por 3 días. Este medicamento es altamente tóxico, por lo que se debe chequear el funcionamiento hepático y renal.
En los pacientes con mal estado general, se comienza la terapia con suramina y luego con el melarsoprol.
Pentamidina. Es considerado actualmente como el medicamento de elección. Se administran 4mg/kg/día por vía intramuscular o endovenosa, con un total de 10 dosis. Es efectiva en la etapa aguda de la infección por T.b gambiense, no así para las cepas resistentes ni para T.b rhodesiense. No atraviesa la barrera encefálica y puede provocar hipotensión, hipoglucemia y en altas dosis es hepatóxica y nefrotóxica.
lunes, 24 de marzo de 2014
Parasitología
La parasitología es la parte de la biología que estudia los fenómenos de dependencia entre los seres vivos. En un sentido amplio, el parasitismo involucra a todos los organismos que pueden vivir sobre los seres humanos. Cualquier organismo, desde un virus (parasitario por definición), hasta la planta o animal más complejo pueden ser parásitos. Pero el campo de la parasitología médica está circusncrito al estudio de protozoarios, helmintos y artrópodos que afectan al hombre.
RAMAS DE LA PARASITOLOGÍA
1. Protozoología: Sarcomastigophora, Apicomplexa, Ciliphora y Microspora.
2. Helmintología:
a) Nemathelminthes.
b) Platihlminthes: clase Cestoidea y Trematoda.
3.Artropodología: Artropoda: clase Insecta, Arachnida y Crustácea.
PARÁSITO
El parásito es aquel ser vivo que vive la totalidad o parte de su existencia en el interior o exterior de otro organismo (hospedero), generalmente más complejo y potente que él, a expensas de cual se nutre y produce o no lesiones aparentes o inaparentes.
PRINCIPALES PARÁSITOS DEL HOMBRE
1.Amebas (intestinales):
a) Entamoeba hstolytica.
b) Entamoeba dispar.
c) Entamoeba hartmanni.
d) Entamoeba coli.
e) Entamoeba polecki.
f) Endolimax nana.
g) Iodoameba butschlii.
h) Blastocystis hominis.
2. Flagelados (intestinales):
a) Giardia lamblia.
b) Chilomastix mesnilii.
c) Dientamoeba fragilis.
d)Trichomoas hominis.
f) Retortamonas intestinalis.
g) Entamoeba gingivalis.
3. Ciliados (intestinales):
a) Balantidium coli.
4. Coccidios (intestinales):
a) Cryptosporidium parvum.
b) Cyclospora cayetanensis.
c) Isospora belli.
d) Sarcocystis hominis.
e) Sarcocystis suihominis.
5.Microsporidios (intestinales):
a) Enterocytozoon bieneusi.
b) Encephalitozoon intestinalis.
6. Esporozoarios de la sangre y los tejidos:
a) Plasmodiun vivax.
b) Plasmodium ovale.
c) Pasmodium malariae.
d) Plasmodium falciparum.
e) Babesia spp.
7.Flagelados de la sangre y lso tejidos:
a) Leishmania (complejo tropica).
b) Leishmania (complejo mexicana).
c) Leishmania (complejo braziliensis).
d) Leishmania (complejo donovani).
e) Leishmania peruviana.
f) Trypanosoma brucei gambiense.
g) Tripanosoma brucei rhodesiense.
h) Trypanosoma cruzi.
i) Tripanosoma rangeli.
8.Amebas de vida libre:
a) Naegleria fowleri.
b) Acanthamoeba spp.
c) Hartmannella spp.
d) Balamuthia mandrillaris.
9.Otros flagelados:
a) Trichomonas tenax.
b) Trichomonas vaginalis.
10.Otros coccidios, esporozoarios y mcrosporidios:
a)Coccidios:
- Toxoplasma gondii.
- Sacocystis lindemanni.
b)Esporozoarios:
- Pneumocystis carinii (reclasificado como un hongo).
c)Microsporidios:
- Nosema conorii.
- Vittaforma corneae.
- Pleistophora.
- Trachipleistophora hominis.
- Encephalitozoon hellem.
- Encephalitozoon cuniculi.
- Encephalitozoon bieneusi.
- Microsporidium.
Nematodos (gusanos redondos)
1.Intestinales:
a) Ascaris lumbricoides.
b) Enterobius vermicularis.
c) Ancylostoma duodenale.
d) Necator americanus.
e) Strongyloides stercoralis.
f) Trichostrongylus ssp.
g) Trichuris trichiura.
h) Capillaria philippinensis.
2.Hísticos:
a) Trichinella spiralis.
b) Toxara canis.
c) Toxocara cati.
d) Ancylostoma braziliense.
e) Ancylostoma caninum.
f) Dracunculus medinensis.
g) Angiostrongylus cantonensis.
h) Angisotrongylus costaricensis.
i) Gnathostoma spinigerum.
j) Anisakis spp.
k) Phocanema spp.
i) Contracaecum spp.
m) Capillaria hepatica.
n) Thelazia spp.
3.Sanguíneos e hísticos:
a) Wuchereria bancrofti.
b) Brugia malayi.
c) Brugia timori.
d) Loa loa.
e) Onchocerca volvulus.
f) Mansonella ozzardi.
g) Mansonella streptocerca.
h) Mansonella pertans.
i) Dirofilaria immitis.
j) Dirofilaria spp.
Cestodos
1.Intestinales:
a) Diphyllobothrium latum.
b) Dipylidium caninum.
c) Hymenolepis nana.
d) Hymenolepis diminuta.
e) Taenia solium.
f) Taenia saginata.
2.Hístico:
a) Taenia solium.
b) Echinococcus granulosus.
c) Echinococcus multilocularis.
d) Multiceps multiceps.
e) Spirometra mansonoides.
f) Diphyllobothrium spp.
Trematodos
1.Intestinales:
a) Fasciolopsis buski.
b) Echinostoma ilocanum.
c) Heterophyes herophyes.
d) Metagonimus yokogawai.
2.Hepáticos y pulmonares:
a) Clonorchis sinensis.
b) Opisthorchis viverrini.
c) Fasciola hepatica.
d) Paragonimus westermani.
e) Paragonimus mexicanus.
f) Paragonimus heterotremus.
g) Paragonimus skrjabini.
h) Paragonimus spp.
3.Sanguíneos:
a) Schistosoma mansoni.
b) Schistosoma haematobium.
c) Schistosoma japonicum.
d) Schistosoma intercalatum.
e) Schistosoma mekongi.
Artrópodos
1.Arácnidos:
a) Escorpiones.
b) Arañas.
c) Garrapatas.
d) Sarcoptes scabiei.
2. Crustáceos:
a) Armilifer armillatus.
b) Linguatuala serrata.
4.Insectos:
a) Piojos (Pediculus, Phthirus).
b) Cucarachas.
c) Hemípteros (Triatoma).
d) Moscas.
e) Mariposas.
f) Mosquitos.
g) Pulgas.
ASOCIACIONES BIOLÓGICAS
Hay varios tipos de ineracciones biológicas en las cuales dos organismos se asocian para vivir. Las más importantes son las siguientes:
1. Parasitismo: este tipo de asociación sucede cuando un ser vivo (parásito) se aloja en otro de diferente especie (hospedero) del cual se alimenta. Por ejemplo, Ascaris lumbricoides, parásitos macho y hembra viven en el interior de otro ser vivo, el hombre, a expensas del cual se derrollan. Se considera, desde el punto de vista biológico, que los mejores adaptados al hospedero son los que menor daño le provocan; por lo tanto, aquellos parásitos que provocan la muerte de sus hospederos son los menos adaptados.
El parasitismo está lejos de ser una condición rara o poco común. Es problable que haya más especies parasitarias que hospederos. Más importante aún, el parasitismo no es una condición anormal ni necesriame4nte patógena.
2.Comensalismo: asociación de dos especies diferentes, donde solo uno de los dos obtiene beneficio, pero ninguna sufre daño; es decir, el parásito deriva todo el beneficio para él, sin ofrecer nada, pero sin causar afectación al hospedero. Por ejemplo, ciertos peces viven adheridos al dorso de los tiburones e ingieren restos que consumen estos; o algunas amebas no patógenas como la Entamoeba coli, en el intestino humano.
3.Mutualismo: asociación de dos especies diferentes para beneficio mutuo. Por ejemplo, protozoos ciliados que degradan la celulosa en el rumen de los rumiantes; así también, un crustáceo de abdomen blando (que vive dentro de la concha de un molusco) y una actinia, que se fija sobre dicha concha. El crustáceo transporta la actinia, esta renueva su medio nutritivo y a su vez lo defiende con una sustancia urticante que segrega.
4.Inqulinismo: ocurre cuando un ser se aloja en otro sin dañarlo y sin depender de él para alimentarse. Por ejemplo, existes peces que viven en el cuerpo de ciertos equinodermos para nutrirse; algunos consideran que la hembra del Schistosoma vive como inquilino en el cuerpo del macho.
5.Simbiosis: asociación íntima entre dos organismos de distintas especies para beneficio mutuo y sin el cual no pueden subsistir. Están unidos tan íntimamente que no pueden vivir separados. Por ejemplo, los comejenes al no poseer enzimas digestivas se asocian con ciertos protozoos que en su tubo digestivo transforman la celulosa en azúcar, y proporcionan alimentos para ambos; el liquen, constituindo por algas y hongos; el alga aporta la clorofila para la síntesis hidrocarbonada y el hongo mantiene la humedad necesaria para la realización de los cambios metabólicos.
HOSPEDERO
Los conceptos de parásito y hospedero (huésped) se condicionan mutuamente; no se puede hablar de uno sin pensar inmediatamente el el otro. El estudio de los hospederos se llama xenología.
Huésped u hospedero. Son aquellos seres (vertebrados e invertebrados) implicados en el ciclo evolutivo de los parásitos a los cuales reciben o alojan; es el animal que recibe el parásito.
Hospedero definitivo(HD). Es aquel que alberga la forma adulta del parásito o en el cual se reproduce sexualmente. Por ejemplo, es el HD del Ascaris lumbricoides.
Hospedero intermediario(HI). Es aquel que alberga las formas larvarias en desarrollo o en el cual se reproduce de manera asexual.Por ejemplo, caracoles del género Lymnaea son denomina activo, mientras queel pasivo aquel que solo sirve de albergue provisional a una larva en tránsito.
Hospedero accidental(HA). Es un hospedero que no se haya involucrado en el ciclo natural de una parasitosis.
Hospedero paraténico o de transporte(HP). Es un hospedero accidental en el cual el parásito no evoluciona, no continúa su ciclo habitual, pero puede sobrevivir alojado en los tejidos. Por ejemplo, el hombre como hospedero paraténico de larvas de moscas; los peces son HP de Gnathostoma spinegerum .
Hospedero habitual(HH). Es el que regularmente y de manera habitual, aloja un parásito determinado.
Hospedero vicariante (HV). Es el que, en condiciones especiales, en ausencia del hospedero habitual sirve de hospedero a un parásito dado.
CICLO EVOLUTIVO (CICLO DE VIDA)
Es el conjunto de procesos, transformaciones o estadios que realiza un parásito para llegar al hospedero, desrrollarse en él y producir formas infectantes que aseguren la supervivencia de la propia especie.
El ciclo de vida más simple es aquel que permite a los parásitos dividrse en el interior de su hospedero, aumentar su número y, al mismo tiempo, producir formas que salgan al exterior para infectar otros nuevos hospedero. Este ciclo existe principalmente en los protozoos. En los helmintos se presentan otros tipos de ciclos que requieren la salida al exterior de huevos o larvas, que en circunstancias propicias de temperatura y humedad llegan a ser infectantes.
En ciclos más complicados existen hospederos intermediarios en los cuales las formas larvarias crecen o se multiplican antes de pasar a los hospederos definitivos.
Los ciclos biológicos comprenden dos tipos básicos:
1.Ciclo directo: el parásito tiene un solo hospedero, a cuyo organismo llega sin intervención de otro
2.Ciclo indirecto: el parásito necesita un hospedero definitivo un hospedero definitivo y uno o más intermediarios.
El dominio de cada uno de los ciclos biológicos de los parásitos le facilita al médico el diagnóstico de las enfermedades infecciosas y, sobre todo, le permite tomar medidas curativas que restauran la salud a sus paciente, así como las medidas preventivas que protejan a la comunidad del surgimiento de nuevo casos.
Fuente Bibliográfia: Microbiología y Parasitología Médicas
Autores principales
Llop Hernández, Alina M.D.
Valdés-Dapena Vivanco, Ma. Margarita M.D Ph.D.
Zuazo Silva, Jorge L. M.D.
RAMAS DE LA PARASITOLOGÍA
1. Protozoología: Sarcomastigophora, Apicomplexa, Ciliphora y Microspora.
2. Helmintología:
a) Nemathelminthes.
b) Platihlminthes: clase Cestoidea y Trematoda.
3.Artropodología: Artropoda: clase Insecta, Arachnida y Crustácea.
PARÁSITO
El parásito es aquel ser vivo que vive la totalidad o parte de su existencia en el interior o exterior de otro organismo (hospedero), generalmente más complejo y potente que él, a expensas de cual se nutre y produce o no lesiones aparentes o inaparentes.
PRINCIPALES PARÁSITOS DEL HOMBRE
1.Amebas (intestinales):
a) Entamoeba hstolytica.
b) Entamoeba dispar.
c) Entamoeba hartmanni.
d) Entamoeba coli.
e) Entamoeba polecki.
f) Endolimax nana.
g) Iodoameba butschlii.
h) Blastocystis hominis.
2. Flagelados (intestinales):
a) Giardia lamblia.
b) Chilomastix mesnilii.
c) Dientamoeba fragilis.
d)Trichomoas hominis.
f) Retortamonas intestinalis.
g) Entamoeba gingivalis.
3. Ciliados (intestinales):
a) Balantidium coli.
4. Coccidios (intestinales):
a) Cryptosporidium parvum.
b) Cyclospora cayetanensis.
c) Isospora belli.
d) Sarcocystis hominis.
e) Sarcocystis suihominis.
5.Microsporidios (intestinales):
a) Enterocytozoon bieneusi.
b) Encephalitozoon intestinalis.
6. Esporozoarios de la sangre y los tejidos:
a) Plasmodiun vivax.
b) Plasmodium ovale.
c) Pasmodium malariae.
d) Plasmodium falciparum.
e) Babesia spp.
7.Flagelados de la sangre y lso tejidos:
a) Leishmania (complejo tropica).
b) Leishmania (complejo mexicana).
c) Leishmania (complejo braziliensis).
d) Leishmania (complejo donovani).
e) Leishmania peruviana.
f) Trypanosoma brucei gambiense.
g) Tripanosoma brucei rhodesiense.
h) Trypanosoma cruzi.
i) Tripanosoma rangeli.
8.Amebas de vida libre:
a) Naegleria fowleri.
b) Acanthamoeba spp.
c) Hartmannella spp.
d) Balamuthia mandrillaris.
9.Otros flagelados:
a) Trichomonas tenax.
b) Trichomonas vaginalis.
10.Otros coccidios, esporozoarios y mcrosporidios:
a)Coccidios:
- Toxoplasma gondii.
- Sacocystis lindemanni.
b)Esporozoarios:
- Pneumocystis carinii (reclasificado como un hongo).
c)Microsporidios:
- Nosema conorii.
- Vittaforma corneae.
- Pleistophora.
- Trachipleistophora hominis.
- Encephalitozoon hellem.
- Encephalitozoon cuniculi.
- Encephalitozoon bieneusi.
- Microsporidium.
Nematodos (gusanos redondos)
1.Intestinales:
a) Ascaris lumbricoides.
b) Enterobius vermicularis.
c) Ancylostoma duodenale.
d) Necator americanus.
e) Strongyloides stercoralis.
f) Trichostrongylus ssp.
g) Trichuris trichiura.
h) Capillaria philippinensis.
2.Hísticos:
a) Trichinella spiralis.
b) Toxara canis.
c) Toxocara cati.
d) Ancylostoma braziliense.
e) Ancylostoma caninum.
f) Dracunculus medinensis.
g) Angiostrongylus cantonensis.
h) Angisotrongylus costaricensis.
i) Gnathostoma spinigerum.
j) Anisakis spp.
k) Phocanema spp.
i) Contracaecum spp.
m) Capillaria hepatica.
n) Thelazia spp.
3.Sanguíneos e hísticos:
a) Wuchereria bancrofti.
b) Brugia malayi.
c) Brugia timori.
d) Loa loa.
e) Onchocerca volvulus.
f) Mansonella ozzardi.
g) Mansonella streptocerca.
h) Mansonella pertans.
i) Dirofilaria immitis.
j) Dirofilaria spp.
Cestodos
1.Intestinales:
a) Diphyllobothrium latum.
b) Dipylidium caninum.
c) Hymenolepis nana.
d) Hymenolepis diminuta.
e) Taenia solium.
f) Taenia saginata.
2.Hístico:
a) Taenia solium.
b) Echinococcus granulosus.
c) Echinococcus multilocularis.
d) Multiceps multiceps.
e) Spirometra mansonoides.
f) Diphyllobothrium spp.
Trematodos
1.Intestinales:
a) Fasciolopsis buski.
b) Echinostoma ilocanum.
c) Heterophyes herophyes.
d) Metagonimus yokogawai.
2.Hepáticos y pulmonares:
a) Clonorchis sinensis.
b) Opisthorchis viverrini.
c) Fasciola hepatica.
d) Paragonimus westermani.
e) Paragonimus mexicanus.
f) Paragonimus heterotremus.
g) Paragonimus skrjabini.
h) Paragonimus spp.
3.Sanguíneos:
a) Schistosoma mansoni.
b) Schistosoma haematobium.
c) Schistosoma japonicum.
d) Schistosoma intercalatum.
e) Schistosoma mekongi.
Artrópodos
1.Arácnidos:
a) Escorpiones.
b) Arañas.
c) Garrapatas.
d) Sarcoptes scabiei.
2. Crustáceos:
a) Armilifer armillatus.
b) Linguatuala serrata.
4.Insectos:
a) Piojos (Pediculus, Phthirus).
b) Cucarachas.
c) Hemípteros (Triatoma).
d) Moscas.
e) Mariposas.
f) Mosquitos.
g) Pulgas.
ASOCIACIONES BIOLÓGICAS
Hay varios tipos de ineracciones biológicas en las cuales dos organismos se asocian para vivir. Las más importantes son las siguientes:
1. Parasitismo: este tipo de asociación sucede cuando un ser vivo (parásito) se aloja en otro de diferente especie (hospedero) del cual se alimenta. Por ejemplo, Ascaris lumbricoides, parásitos macho y hembra viven en el interior de otro ser vivo, el hombre, a expensas del cual se derrollan. Se considera, desde el punto de vista biológico, que los mejores adaptados al hospedero son los que menor daño le provocan; por lo tanto, aquellos parásitos que provocan la muerte de sus hospederos son los menos adaptados.
El parasitismo está lejos de ser una condición rara o poco común. Es problable que haya más especies parasitarias que hospederos. Más importante aún, el parasitismo no es una condición anormal ni necesriame4nte patógena.
2.Comensalismo: asociación de dos especies diferentes, donde solo uno de los dos obtiene beneficio, pero ninguna sufre daño; es decir, el parásito deriva todo el beneficio para él, sin ofrecer nada, pero sin causar afectación al hospedero. Por ejemplo, ciertos peces viven adheridos al dorso de los tiburones e ingieren restos que consumen estos; o algunas amebas no patógenas como la Entamoeba coli, en el intestino humano.
3.Mutualismo: asociación de dos especies diferentes para beneficio mutuo. Por ejemplo, protozoos ciliados que degradan la celulosa en el rumen de los rumiantes; así también, un crustáceo de abdomen blando (que vive dentro de la concha de un molusco) y una actinia, que se fija sobre dicha concha. El crustáceo transporta la actinia, esta renueva su medio nutritivo y a su vez lo defiende con una sustancia urticante que segrega.
4.Inqulinismo: ocurre cuando un ser se aloja en otro sin dañarlo y sin depender de él para alimentarse. Por ejemplo, existes peces que viven en el cuerpo de ciertos equinodermos para nutrirse; algunos consideran que la hembra del Schistosoma vive como inquilino en el cuerpo del macho.
5.Simbiosis: asociación íntima entre dos organismos de distintas especies para beneficio mutuo y sin el cual no pueden subsistir. Están unidos tan íntimamente que no pueden vivir separados. Por ejemplo, los comejenes al no poseer enzimas digestivas se asocian con ciertos protozoos que en su tubo digestivo transforman la celulosa en azúcar, y proporcionan alimentos para ambos; el liquen, constituindo por algas y hongos; el alga aporta la clorofila para la síntesis hidrocarbonada y el hongo mantiene la humedad necesaria para la realización de los cambios metabólicos.
HOSPEDERO
Los conceptos de parásito y hospedero (huésped) se condicionan mutuamente; no se puede hablar de uno sin pensar inmediatamente el el otro. El estudio de los hospederos se llama xenología.
Huésped u hospedero. Son aquellos seres (vertebrados e invertebrados) implicados en el ciclo evolutivo de los parásitos a los cuales reciben o alojan; es el animal que recibe el parásito.
Hospedero definitivo(HD). Es aquel que alberga la forma adulta del parásito o en el cual se reproduce sexualmente. Por ejemplo, es el HD del Ascaris lumbricoides.
Hospedero intermediario(HI). Es aquel que alberga las formas larvarias en desarrollo o en el cual se reproduce de manera asexual.Por ejemplo, caracoles del género Lymnaea son denomina activo, mientras queel pasivo aquel que solo sirve de albergue provisional a una larva en tránsito.
Hospedero accidental(HA). Es un hospedero que no se haya involucrado en el ciclo natural de una parasitosis.
Hospedero paraténico o de transporte(HP). Es un hospedero accidental en el cual el parásito no evoluciona, no continúa su ciclo habitual, pero puede sobrevivir alojado en los tejidos. Por ejemplo, el hombre como hospedero paraténico de larvas de moscas; los peces son HP de Gnathostoma spinegerum .
Hospedero habitual(HH). Es el que regularmente y de manera habitual, aloja un parásito determinado.
Hospedero vicariante (HV). Es el que, en condiciones especiales, en ausencia del hospedero habitual sirve de hospedero a un parásito dado.
CICLO EVOLUTIVO (CICLO DE VIDA)
Es el conjunto de procesos, transformaciones o estadios que realiza un parásito para llegar al hospedero, desrrollarse en él y producir formas infectantes que aseguren la supervivencia de la propia especie.
El ciclo de vida más simple es aquel que permite a los parásitos dividrse en el interior de su hospedero, aumentar su número y, al mismo tiempo, producir formas que salgan al exterior para infectar otros nuevos hospedero. Este ciclo existe principalmente en los protozoos. En los helmintos se presentan otros tipos de ciclos que requieren la salida al exterior de huevos o larvas, que en circunstancias propicias de temperatura y humedad llegan a ser infectantes.
En ciclos más complicados existen hospederos intermediarios en los cuales las formas larvarias crecen o se multiplican antes de pasar a los hospederos definitivos.
Los ciclos biológicos comprenden dos tipos básicos:
1.Ciclo directo: el parásito tiene un solo hospedero, a cuyo organismo llega sin intervención de otro
2.Ciclo indirecto: el parásito necesita un hospedero definitivo un hospedero definitivo y uno o más intermediarios.
El dominio de cada uno de los ciclos biológicos de los parásitos le facilita al médico el diagnóstico de las enfermedades infecciosas y, sobre todo, le permite tomar medidas curativas que restauran la salud a sus paciente, así como las medidas preventivas que protejan a la comunidad del surgimiento de nuevo casos.
Fuente Bibliográfia: Microbiología y Parasitología Médicas
Autores principales
Llop Hernández, Alina M.D.
Valdés-Dapena Vivanco, Ma. Margarita M.D Ph.D.
Zuazo Silva, Jorge L. M.D.
Marcadores:
Artropodología,
ciclo,
clasificación,
estudio,
glosário,
Helmintología,
hospedero,
Infección,
Microbiología,
Parasitologia,
Protozoología
sábado, 22 de marzo de 2014
Protozoarios-Trichomona vaginalis (tricomoniosis)
Son protozoarios flagelados que parasitan al hombre (tracto digestivo o reproductor) y diversos animales. No desarrollan quistes, existiendo solamente en su forma vegetativa: el trofozoíto. Este fagocita bacterias, leucocitos y enterocitos para su supervivencia.
De las tres especies que parasitan al humano (T. hominis, T.tenax y T. vaginalis) solo Trichomona vaginalis es patógena. Las otras dos son comensales de boca y colon.
La tricomonosis es una enfermedad de transmisión sexual (ETS) exclusiva del humano.
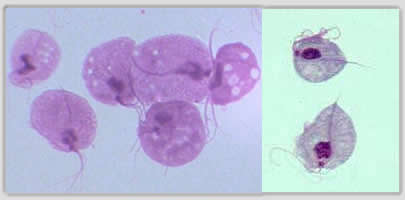
Morfología
Recordar que solo existen en su forma vegetativa, el trofozoíto.
Posee núcleo, un citostoma con un grupo de cuatro flagelos libres anteriores y un flagelo adicional sobre la porción externa de una membrana ondulante. Además cuenta con un axostilo posterior, siderosomas e hidrogenosomas. Se reproducen asexuadamente por fisión binaria.
Las tricomonas evaden la respuesta inmune por una enzima, la cisteína-proteasa, que cliva inmunoglobulinas. Además, esta enzima es capaz de producir daño celular.
De las tres especies que parasitan al humano (T. hominis, T.tenax y T. vaginalis) solo Trichomona vaginalis es patógena. Las otras dos son comensales de boca y colon.
La tricomonosis es una enfermedad de transmisión sexual (ETS) exclusiva del humano.
Morfología
Recordar que solo existen en su forma vegetativa, el trofozoíto.
Posee núcleo, un citostoma con un grupo de cuatro flagelos libres anteriores y un flagelo adicional sobre la porción externa de una membrana ondulante. Además cuenta con un axostilo posterior, siderosomas e hidrogenosomas. Se reproducen asexuadamente por fisión binaria.
Las tricomonas evaden la respuesta inmune por una enzima, la cisteína-proteasa, que cliva inmunoglobulinas. Además, esta enzima es capaz de producir daño celular.
Se debe recordar que no existe la forma quística de este parasito
Epidemiología
T. vaginalis de flora normal de uretra y vagina en la mujer y próstata, vesículas seminales y uretra en el hombre. La transmisión de esta parasitosis es por contacto sexual exclusivamente (debido a que no presenta la forma de resistencia quística). La tricomonosis presenta mayor incidencia durante el embarazo (por la presencia de moco, secretado por un cérvix hipertófico, hiperactivo y blando) y disminuye su incidencia en la menopausia y pacientes prepuberales (en ambos casos debido a los cambios de pH vaginal).
La mayor incidencia en la mujer en entre los 20 y 50 años (debido a la mayor actividad sexual) y en la raza negra.
Se ha registrado una mayor incidencia de infección con N. gonorrhoeae cuando coexisten los dos microorganismo. Si existe la incidencia baja al haber tricomonosis.
En el hombre es menos frecuente, siendo favorecida por aumento de pH seminal, presencia de sangre menstrual y/o mucus cervical uterino.
Ciclo evolutivo
Al ingresar a la vagina, las tricomonas se reproducen dañando el epitelio vaginal con posterior descamación. Debido a esto, se produce un infiltrado leucocitario e intensa inflamación local, que abarca clítoris, orificio uretral y glándulas vestibulares.
Clínica
La sintomalogía es de aparición más frecuente en las mujeres. La presencia o no de clínica tiene que ver con la carga parasitaria y el pH vaginal. Las formas clínicas en la mujer son: forma asintomática, forma subclínica y vulvaginitis (que puede ser aguda o crónica).
- Vulvovaginitis: Tras un período de incubación de 4-28 días, aparecen leucorrea (flujo balnquecino, mal oliente y con presencia de leucocitos), vulvitis, prurito (picazón) vulvar y disuria (dolor miccional).
Se deben plantear e diagnóstico diferencia con infecciones bacteriana y micoticas producidas por N. gonorrhea trachomatis, Candida albicans,Gardnerella vaginalis, Mycoplasma hominis y reaplasma realiticum |
Diagnóstico
Debido a que la clínica es inespecífica (por las posibilidades de infección con otros microorganismo), se prefieren los métodos directos e indirectos para el diagnóstico.
- Métodos directos
Papanicolau.
Examen directo en fresco de muestras de orina. Este método es muy útiles en del sexo masculino.
Cultivo:es el método más sensible y se emplea cuando fracasan los métodos directos de visualización
- Métodos indirectos
- IFD (requiere una cierta cantidad dde tricomonas para ser positivo).
- PCR (tiene una sensisibilidad del 96% y una especificidad del 100%
| Bibliografía: Dorfmann y Passerelli Introducción a la microbiología médica |
Marcadores:
ciclo,
contacto,
diagnóstico,
epidemiología,
hombre,
infectar,
mujer,
órgano feminino,
órgano masculino,
penis,
protozoarios,
sexo,
sexuada,
sexual,
Trichomonas vaginalis,
vagina
jueves, 20 de marzo de 2014
Protozoarios-Balantidium coli (balantidiasis)
Es un protozoario ciliado que habita en el intestino grueso del cerdo, que constituye el reservorio natural de la infección. Su presencia en el humano es rara y se caracteriza por infecciones intestinales con sintomalogía similar a la de una amebiasis. B. coli es el más grande de los protozoarios intestinales.
Morfologia
EpidemiologíaMorfologia
- Trofozoíto: Es ovoide y grande. Tiene metabolismo aeróbico y utiliza bacterias como fuente de hierro. Posee, en su extremo anterior, una abertura por donde incorpora alimentos: el citostoma El "cuerpo" se encuentra cubierto por cilios que le permiten traladarse activamente. En el extremo posterior aparece una vacuola con elementos de excreción, que descarga a una abertura o ano llamada citopigio. Cuenta con dos núcleos, macro y micronúcleo y se reproduce asexuadamente por fisión binaria. Sin embargo, pueden llegar a tener una forma de reproducción sexual al intercambiar, en ocasiones, material cromosómico sin que haya reproducución alguna.
- Quiste: Es redondeado y contiene un solo trofozoíto con cilios y macro y micronúcleo en su interior
La infección es mantenida en la naturaleza por cerdos infectados. El hombre ingresa en el ciclo como hospedero accidental. La vía de infección es oral (fecalismo), por ingestión de aguas, y alimentos contaminados con quistes de B. coli.
Ciclo evolutivo
El ingiere quistes que, al llegar al estómago e intestino proximal, se digieren y permiten la liberación de trofozoítos. Estos últimos, si encuentran condiciones favorables, comenzarán a dividirse. Las lesiones (tanto químicas como mecánicas) que producen son ulcerativas y similares a las producidas por E. histolytica y bacterias productoras de úlceras intestinales. El sitio más afectado es el rectosigmoides, seguido por ciego y colon en general. En ocasiones los parásitos pueden provocar úlceras profundas que perforan la pared intestinal con la consecuente peritonitis. En condiciones adversas, los trofozoítos de B. coli, se enquistan. El hospedero eliminará tanto quistes como trofozoítos en materia fecal, contaminado aguas y suelos.
Clínica
Existe diferentes formas clíncias, pudiendo ser asintomática en un número importante de casos. Las formas sintomáticas son: la balantidiosis aguda (disentería balantidiana) y la balantidiosis crónica.
- Balantidiosis aguda: Se presenta como un cuadro de diarrea aguda, como moco, sangre, pujo y tenesmo (disentería), simulando una disentería amebiana o bacilar (bacteriana). Estas manifestaciones se acompañan de afección del estado general del paciente (fiebre, astenia , malestar general, deshidratación). El parásito se ubica en el rectosigmoides.
- Balantidiosis crónica: Puede presentarse como cuadros diarreicos con moco, sangre y dolor abdominal, o como molestias intestinales, dolores abdominales inespecífico, náuseas y vómitos.
Se ultilizan métodos drectos como detección de trofozaítos en heces fresas y endoscopías o detección de quistes en exámenes coproparasitológicos seriados.
El diagnóstico diferencial de la forma se debe plantear con la amebiasis.
Un "quiste" de Balantidium coli
Balantidium coli tal como se observa en una muestra de heces. E
l organismo está rodeado de cilios.

Bibliografía: Dorfman/Passarelli del libro Introducción a la Microbiologia Médica.
Marcadores:
amebiasis,
Balantidium Coli,
ciclo,
clínica,
diagnóstico,
epidemiología.,
examen,
Infección,
Parasitologia,
Parasitos,
patología,
protozoarios,
quistes,
tratamiento,
trofozoítos
Protozoarios-Giardia intestinalis (giardisis)
G.Intestinales (también llamada G. Lamblia y G.duodenalis) produce infecciones gastrointestinales agudas o crónicas especialmente en niños e inmunodeprimidos. En adultos produce, generalmente, infecciones asintomáticas. La giardiasis puede llevar a síndromes de malabsorción.
Morfología
Es una infección frecuente en áreas rurales de América Latina. El mecanismo de infección es el fecalismo (vía fecal-oral).
Ciclo evolutivo
El ciclo comienza cuando el quiste ingresa al hospedero por vía oral. Frente a la acidez gástrica y el rápido aumento del pH en el duodeno se produce la desenquistación y se liberan los trofozoítos, que se fijan por medio de sus discos suctorios a las vellosidades duodenales y se multiplican activamente por fisión binaria. En las vellosidades se produce daño y muerte de los enterocitos, con liberación de los mismos a la luz intestinal. Frete a la depleción de enterocitos de las velellosidades aumenta el recambio celular, pbalndo la vellosidad de células inmaduras incapaces de natener correctamente los procesos enzimáticos y de transporte. Esto determinará una incorrecta absorción de nutrientes (traducido clínicamente por un síndrome de malabsorción). Si las condiciones del medio se tornan adveras, algunos trofozoítos se diferencian a prequistes (con 2 núcleos) y luego a quistes maduros, que son eliminados por heces. El portador humano puede liberar grandes cantidades de quistes, que mantienen su capacidad infectante durante 3-12 meses en agua clorada cuando la temperatura ambiente es baja, por día, contaminando verduras y agua. Esto mantiene esta parasitosis en la naturaleza.
Clínica
La presencia o no de sintomatología depende de la carga parasitaria, la virulencia, el estado inmunológico del hospedero, la motilidad intestinal y la acidez gástrica. Se puede decir que el adulto, generalmente, es portador asintomático. La infección se manifiesta clínicamente en adultos inmunocomprometidos y niños.
Interacción con el hospederoMorfología
- Trofozoíto: Es la forma vegetativa del parásito. Posee dos núcleos grandes y vesiculados con nucléolos prominentes. Además posee cuerpos mediales o parabasales y cuatro pares de flagelos que le otorgan movilidad. En la cara ventral posee un disco suctorio con el cual, la Giardia incorpora sales biliares y líquidos. Se divide por fisión binaria y se desarrolla principalmente en el medio alcalino del tracto gastrointestinal superior. Debido a que son muy lábilies fuera del hospedero, no se lo considera el elemento-infectante.
- El trofozoíto vive en el intestino delgado proximal (duodeno y porción proximal de yeyuno).
- Quistes: Constituyen los elementos infectantes debido a la resistencia que presentan frente a las condiciones adversas del medio fuera del hospedero. Son ovalados y muy refringentes al microscopio óptico. Poseen una doble pared, cuatro núcleos ( quistes tetranucleados) y cuatro cuerpos mediales o parabasales. Los quistes resisten la cloración y perpetúan la enfermedad.
Es una infección frecuente en áreas rurales de América Latina. El mecanismo de infección es el fecalismo (vía fecal-oral).
Ciclo evolutivo
Clínica
La presencia o no de sintomatología depende de la carga parasitaria, la virulencia, el estado inmunológico del hospedero, la motilidad intestinal y la acidez gástrica. Se puede decir que el adulto, generalmente, es portador asintomático. La infección se manifiesta clínicamente en adultos inmunocomprometidos y niños.
- Fase aguda: Se presenta con náuseas, vómitos, diarrea acuosa y epigastralgia (dolor en el epigastrio). Además puede haber meteorismo y anorexia.
- Fase crónica: Se presenta como una diarrea crónica de características malabosrtivas: Puede aparecer lientería (posibilidad de reconocer los alimentos ingeridos) y, acompañado la anorexia y los dolores, gran pérdida de peso. Este cuadro puede llegar a constituir un síndrome de malabsorción intestinal.
La producción de anticuerpos IgG mediaría la destrucción de los trofozoítos por ADCC, mientras que anticuerpos de tipo IgM por activación de la vía clásica del complemento controlarían la infección. Además la IgA secretoria local, dificultaría la adhesión de las Giardias al epitelio intestinal.
Diagnóstico
biografía: Dorfmann y Passarelli Introducción a la microbiología médica
Marcadores:
amebiasis,
ciclo,
clínica,
diagnóstico,
epidemiología.,
examen,
Giardia lamblia,
Infección,
Parasitologia,
Parasitos,
patología,
protozoarios,
quistes,
tratamiento,
trofozoítos
Suscribirse a:
Entradas (Atom)